Histoire de la chirurgie de la névralgie faciale
Les douleurs atroces du « tic douloureux » ont contraint les chirurgiens à s’y intéresser bien avant la naissance de la neurochirurgie. Ces interventions, dans un premier temps, chercheront à interrompre les fibres sensitives incriminées. Au niveau des branches, déjà, par les neurotomies, puis du ganglion — la gassérectomie — et enfin à la racine du trijumeau avec la neurotomie rétrogassérienne par voie temporale ou sous-occipitale. Toujours dans cette logique lésionnelle, la voie percutanée sera également explorée. La neurolyse alcoolique, l’alcoolisation ou la thermocoagulation du ganglion de Gasser chercheront à reproduire les résultats des interventions précédentes sans les risques d’une chirurgie ouverte. Parmi ces techniques percutanées, la compression par ballonnet et la thermocoagulation appartiennent à l’arsenal thérapeutique actuel. Une meilleure compréhension de la physiopathologie aboutira, dans un second temps, à un nouveau geste — conservateur cette fois — conservateur : la décompression vasculaire microchirurgicale. Plus récente et non invasive, la radiochirurgie visant la racine du nerf trouve aujourd’hui sa place au côté de la décompression vasculaire et des gestes percutanés en cas d’échecs du traitement médicamenteux de la névralgie faciale.
Introduction
La prise en charge chirurgicale de la névralgie faciale tient une place à part dans la chirurgie de la douleur. Le cheminement des idées dans le traitement du « tic douloureux » obéit à une logique distincte des autres douleurs chroniques. Alors que ces dernières résultent de lésions tissulaires, parfois graves, la névralgie faciale essentielle intervient sans que l’on ne décèle de lésion. Cette « maladie fort grave, et pourtant compatible avec toutes les apparences de la santé la plus florissante, n’a peut-être pas une seule fois causé directement la mort, mais l’a bien souvent fait désirer par les douleurs atroces qui l’accompagnent et le découragement moral qui l’a suit » écrivait D. Halliday en 1832 [1]. C’est probablement l’intensité de ces crises survenant chez des individus « en bonne santé » autant que la difficulté à les soulager qui, très tôt, ont incité les chirurgiens à se pencher sur cette maladie née « pour le tourment des médecins aussi bien que pour celui des malades » ajoutait le praticien français [1]. C’est à un chirurgien, Nicolas André, que l’on doit, en 1756, la description du « tic douloureux » [2] telle une entité clinique à part entière distincte d’autres conditions douloureuses du visage [3]. Certes, des nosographies — celles de J-L. Bausch en 1671 ou de J. Locke en 1677 — avaient précédée celle du chirurgien à la cour de Louis XIV. Mais que ce soit l’Allemand ou le Britannique, aucun de ces praticiens n’y avait vu une maladie en soi, le chirurgien de Versailles, lui, considérait que ces crises provenaient de la compression périphérique du nerf trijumeau par des adhésions [4].
La chirurgie ouverte
Les neurotomies périphériques
André confia deux de ses patients souffrant de névralgie de la branche orbitaire à Maréchal, chirurgien du Roi, pour une neurectomie [5]. Ces interventions furent des « échecs sanglants » et l’amenèrent à proposer, ultérieurement, une lever des adhésions par l’application d’un caustique — l’eau mercurielle — sur le nerf [6]. Estimant que les récurrences de la douleur provenaient, à nouveau, de la compression par une fermeture précoce de la plaie André s’opposera à cette cicatrisation par une « pierre de cautère ». Les soulagements obtenus par ce geste — brûlant le nerf — seront confirmés par ses contemporains [6]. En revanche, les autres tentatives de neurectomies infraorbitaires des Français Veillard et Dussans, en 1768, furent jugées infructueuses [5]. Malgré tout, en 1832, dans sa remarquable monographie sur les névralgies de la face, Halliday déclarera « la section du nerf affectée de névralgie [est] l’un des moyens les plus puissants, ou même les plus efficaces de tous » [1]. Toutefois, le neurologue réservera ces interventions de « section, de résection ou de cautérisation » à trois terminaisons : les rameaux frontaux, sous-orbitaires et mentonniers. Un siècle plus tard, au sujet de ces gestes, Leriche tempèrera « nous devons répandre partout cette constatation de fait que les neurotomies et neurectomies périphériques n’ont pas de succès durable à leurs actifs. Elles ont eu autrefois une grande vogue. On crut sincèrement qu’elles allaient tout guérir, surtout après que Thiersch eut substitué l’arrachement à la neurotomie » [7].
La gassérectomie
![Fig. 1 — L’intervention de W. Rose permettant d’accéder au foramen ovale après dissection du nerf mandibulaire [12]](https://image.jimcdn.com/app/cms/image/transf/dimension=445x1024:format=png/path/sc2475004ea3c94e2/image/i3ea9ef7041115d73/version/1559475996/image.png)
En 1856, J-M. Carnochan émit l’hypothèse que la «matière grise du ganglion de Gasser peut être considérée comme un générateur nerveux, telle une batterie galvanique, […] tandis que les branches périphériques, sous l'influence de ce ganglion malade, conduisent la décharge accumulée. Je crois, dans ces conditions, que la clé du traitement chirurgical réside dans l'ablation du ganglion» [8]. Ce chirurgien new-yorkais, disséquera le nerf maxillaire et, au travers du sinus du même nom, procédera à l’ablation d’une partie du ganglion [9]. Cette gassérectomie partielle, quoique relativement délabrante, permit la guérison de ses trois opérés. À Londres, au King’s College, en 1890, W. Rose reprendra le principe de cette intervention, mais selon un abord différent : le foramen ovale (Fig. 1). Après Rose, V. Horsley, par voie intradurale [10], puis F. Hartley par voie extradurale [11] amélioreront la gassérectomie grâce à l’abord temporal. « L’ablation du ganglion parut bientôt le remède héroïque de la névralgie du trijumeau, mais seuls des opérateurs exceptionnels osaient aborder cette chirurgie » se souvient Leriche qui évaluera la mortalité du geste entre « quinze et 25% dans les meilleures mains » [7]. « Un mort sur quatre opérés ! Un borgne sur quatre survivants ! Le bilan était peu enthousiasmant et il fallait une rude foi pour persévérer ». Cette mortalité et les fréquentes kératites, que pointe le père la chirurgie de la douleur, eurent raison de la gassérectomie avant même que les progrès de la neurochirurgie eussent pu la rendre moins dangereuse.
La neurotomie rétrogassérienne

C’est le danger oculaire qui incita, dès 1898, le neurologue G. Spiller à proposer la section de la racine plutôt que la gassérectomie, car « Magendie et Claude Bernard, explique Leriche, avaient en effet établi que les conséquences de la section du trijumeau n’étaient pas les mêmes pour l’œil suivant qu’elle portait avant ou après le ganglion » [7]. Suivant cette proposition, H. Frazier, son collègue chirurgien à Philadelphie, réalisera en 1901 la première neurotomie rétrogassérienne par voie sous-temporale extradurale (Fig. 2) [13]. Cette intervention — dite de « Spiller-Frazier » — offrit, semble-il, d’excellents résultats sur la douleur, mais au prix d’importantes séquelles paresthésiantes. Frazier raffinera son geste en se bornant à une neurotomie partielle qui préservera la portion supérieure de la racine du nerf [14]. En épargnant le contingent ophtalmique, chaque fois que le patient ne présentait pas de crise dans le territoire du nerf ophtalmique (V1), le neurochirurgien américain réduira les complications liées aux anesthésies cornéennes. Frazier cherchera également à préserver le contingent moteur du nerf. Avant-gardiste, il recourra, dès 1921, à la stimulation peropératoire : l’objectif étant de conserver le contingent du nerf qui — au contact de l’électrode — induit une contraction temporale [15].
![Fig. 3 — Le ganglion de Gasser et le trajet des différents contingents selon Guillaume [17]](https://image.jimcdn.com/app/cms/image/transf/dimension=445x1024:format=png/path/sc2475004ea3c94e2/image/i1e4e1bd76738ea31/version/1559476664/image.png)
En France, « c’est J-M. Guillaume, nous rappelle G. Mazars, qui a véritablement institué dés 1947 la neurotomie partielle sélective par voie temporale comme méthode systématique en remplacement de la neurotomie totale de Spiller-Frazier » [16]. Le chirurgien de la Salpêtrière perfectionna le geste en limitant, à son tour, la section de la racine au seul contingent impliqué dans la névralgie. Pour cela un abord directement en arrière du ganglion de Gasser s’avéra nécessaire, car « c’est là en effet, précise Guillaume, le seul niveau auquel on peut pratiquer avec certitude une section partielle de l’un quelconque de contingents de la racine. Plus en arrière, en effet, la torsion des fibres s’ébauche et le caractère systématique du dispositif ne permet plus, à coup sûr, une section partielle » (Fig. 3) [17].

La neurotomie trigéminale par voie sous-occipitale
En 1920, guidée par l’idée qu’une section sélective l’emportait sur la neurotomie totale, W. Dandy, prônera un abord postérieur de ce nerf — entre le lobe cérébelleux et l’os — par une voie intradurale (Fig. 4) [18]. L’élève de Cushing donnera comme avantage à cette section des « deux tiers postéro-externe de la racine du trijumeau » — outre le risque moindre de kératite neuro-paralytique et le respect de la motricité — la possibilité de découvrir et d’enlever une tumeur dont la névralgie serait le symptôme. Plus tard, une meilleure compréhension de l’anatomie précisera la section nerveuse à la racine sensitive (pars major) juste au niveau de son émergence protubérantielle épargnant de ce fait la racine motrice (pars minor) des muscles masticateurs ainsi que les émanations de la sensibilité cornéenne (pars intermediaris). Tenants du geste de Frazier et partisans de celui Dandy s’opposeront durant une vingtaine d’années. Les premiers, comme Guillaume, prônant cette intervention extradurale « que même les malades très âgés ou déficients peuvent supporter » tandis que les seconds argüant, à partir des années soixante, de l’introduction de la magnification optique et d’une meilleure compréhension de la portion juxta-protubérantielle du trijumeau pour améliorer la sélectivité de la section.
La tractotomie bulbaire trigéminale
![Fig. 5 – Incision du bulbe dans la tractotomie trigéminale de Sjöquist, d’après [17]. X : nerf pneumogastrique, XI : nerf spinal](https://image.jimcdn.com/app/cms/image/transf/dimension=391x1024:format=png/path/sc2475004ea3c94e2/image/i4bbc32b9702913aa/version/1559476888/image.png)
Après les branches périphériques, le ganglion puis la racine postérieure, l’intérêt des chirurgiens continuera sa remontée vers le tronc cérébral. À Stockholm, en 1937, O. Sjöquist [19] préconisera, au niveau du bulbe , l’interruption des « fibres de la branche descendante bulbo-spinale du trijumeau […] dévolues aux sensibilités douloureuses et thermiques » [17]. Pour ce faire, l’élève d’Olivecrona réalise une trépanation sous-occipitale exposant la face latérale du bulbe. Le lobe cérébelleux est ensuite récliné afin de visualiser la racine inférieure du pneumogastrique — repère essentiel — puis Sjöquist pratique une incision juste au-dessous de la racine de ce nerf (Fig. 5). L’Américain F. Grant [20] puis le Tchèque Z. Kunc [21] affineront la localisation de cette section. Néanmoins, la persistance d’un risque de complication oculaire et surtout le repérage délicat — requérant l’examen peropératoire de la sensibilité — d’une section au niveau du bulbe amèneront à délaisser ce geste [22].
Dandy — mais également le Suédois H. Olivecrona [23] — avait déjà remarqué que la névralgie pouvait résulter d’une compression. Le Danois, P. Taarnhøj, émit l’hypothèse que la névralgie faciale dite « essentielle » pouvait résulter d’une compression par striction de la dure-mère au niveau du cavum de Meckel [24]. En 1952, ce chirurgien de Copenhague entreprit de traiter les malades souffrant de cette affection par une ouverture de la dure-mère au niveau du cavum. À la même époque, à Pasadena, C. Shelden, eut un raisonnement différent : il estimait que les douleurs provenaient plutôt d’une constriction des branches périphériques au travers des foramens ovale ou rond [25]. Chez une dizaine de patients, il réalisa, par voie temporale, un fraisage de ces orifices. Trois ans plus tard, constatant ses bons résultats et prenant connaissance de ceux de son collègue Danois — également satisfaisants — le chirurgien Californien chercha un dénominateur commun à ces deux interventions. Il en conclura que le traumatisme peropératoire du ganglion pouvait être à l’origine de cette amélioration. Dans une publication intitulée « La compression plutôt que la décompression dans la névralgie du trijumeau » Shelden préconisera une compression, par martèlement, de la racine postérieure [25]. Cette nouvelle procédure aura l’avantage de connaitre peu de complications malheureusement ses bons résultats ne se maintiendront pas dans le temps [15].
La décompression vasculaire microchirurgicale
L’idée qu’une compression du trijumeau — ou de sa racine postérieure — puisse être à l’origine du tic douloureux continuera de faire son chemin. À la fin des années soixante, l’avènement du microscope au bloc opératoire amènera de nouvelles découvertes. Empruntant la voie de Dandy, P. Janetta remarquera, grâce à cette magnification optique, la fréquence anormale d’un conflit vasculaire au contact de la racine postérieure. Dandy, quelques années auparavant avaient déjà observé la même anomalie « dans de nombreux cas le nerf est comprimé ou coudé par une artère. C’est, je crois, la cause du tic douloureux » [26]. Néanmoins le célèbre chirurgien du Johns Hopkins Hospital ne poussera pas la logique à son terme : lever la compression. C’est W. Gardner qui fut le premier, en 1959, à effectuer cette décompression de la racine sensitive du trijumeau en éloignant l’artère du nerf sans pratiquer de section de la racine nerveuse [27]. En 1967, P. Janetta — utilisant la voie sous temporale transtentorielle — avait remarqué la présence d’une artère comprimant la racine qu’il libera en sectionnant l’arachnoïde, il pratiqua ensuite une rhizotomie partielle ou totale de la portion majeure [28]. En 1969, à l’occasion d’un symposium de microneurochirurgie à Montréal, il assista à une démonstration opératoire de la voie sous-occipitale par J. Hardy qui l’utilisait depuis 1962 [29]. Convaincu d’une meilleure exposition par cette approche, le neurochirurgien de Pittsburgh, décida de l’utiliser désormais pour pratiquer la décompression du trijumeau [30]. Par ses excellents résultats cliniques et ses rares complications, cette technique conservatrice s’imposera, progressivement, comme l’intervention de référence dans le traitement de la névralgie faciale essentielle. Ajoutons à cela, qu’à partir de 1962, l’apparition de la Carbamazépine — efficace chez plus de 90% des patients — contribuera à rendre inacceptables les complications (paresthésies faciales, anesthésies cornéennes et autres déficits masticatoires) des anciens gestes lésionnels [31]. Par la suite, Hardy modifiera la technique de Janetta en adoptant la voie rétro-mastoïdienne tandis que le français M. Sindou contribuera à codifier la technique que l’on connaît aujourd’hui [32].
Les techniques percutanées
Avant le début du vingtième siècle, l’issu d’un geste de neurochirurgie demeurait hasardeux et le pronostic vital se devait d’être engagé pour qu’une trépanation soit envisagée. Le fait que la névralgie faciale menait souvent au suicide — même parmi les « âmes les mieux trempées » déplorait Leriche — incita nous l’avons vu, dès 1754, les chirurgiens à s’y intéresser. Néanmoins, en raison de ces risques, qui ne diminueront véritablement qu’avec H. Cushing, l’alternative d’un geste percutanée sera très tôt considérée.
Les neurolyses alcooliques
À la fin du XIXe siècle, l’Américain R. Bartolow [33] puis l’allemand G. Neuber [5] proposeront à la place de la neurotomie périphérique l’injection de chloroforme puis d’acide osmique. Très vite, ces produits seront remplacés par les injections neurolytiques d’alcool. « Imaginées par Pitres et Verger d’une part, par Schloesser, d’autre part, étudié avec soin par Lévy et Beaudouin, [l’alcoolisation] eu des heures de grande vogue » écrira Leriche [7]. Au sujet de ces injections d’alcool — habituellement dans le trou mentonnier, le canal sous-orbitaire et dans le nerf sus-orbitaire — J-M. Guillaume mettra en garde « [ce] sont des interventions faciles et efficaces un certain temps, à condition d’être effectuées à propos et dans une forme localisée de névralgie ; leur efficacité dépasse rarement une année » [17]. Les alcoolisations des nerfs sus et sous orbitaires demeurent aujourd’hui encore pratiquées par quelques équipes dans une indication précises : l’allodynie dans le territoire de ces nerfs — relativement fréquente dans l’évolution des névralgies du trijumeau — en particulier chez les personnes âgées ou les patients souffrant de sclérose en plaque .
L’alcoolisation du ganglion de Gasser
Après ces premières chémo-neurolyses, remontant à 1883, et suivant un cheminement d’idée voisin de celui que connut la chirurgie ouverte, l’intérêt se déplaça vers le ganglion de Gasser. Le Britannique W. Harris, en 1910, sera le premier à injecter une solution alcoolique dans cette structure [34]. Le chirurgien allemand, F. Härtel, popularisera le geste en simplifiant et en codifiant son abord : le trocart sera introduit au travers de la joue puis du foramen ovale [35]. Deux ans plus tard, L. Pollock renforcera la sécurité du geste grâce à un contrôle fluoroscopique [36]. L’injection, quoique relativement aveugle la diffusion du produit neurolytique gagnant parfois les espaces sous-arachnoïdiens, connaîtra, un temps, le succès. Les progrès de la neurochirurgie ne tarderont pas à offrir une alternative plus sure. Leriche déclarera au sujet de ces alcoolisations « c’est assez difficile et quelque peu dangereux, puisque Härtel lui-même n’obtient pas toujours l’anesthésie espérée et compte 25 p. 100 de kératite. Je ne crois pas que ce procédé puisse se généraliser » [7]. Guillaume, De Sèze et Mazars, plus tard, emboîteront le pas « la fréquence des lésions oculaires et, plus spécialement, de la "kératite neuro-paralytique" est incomparablement plus grande après une alcoolisation du ganglion de Gasser qu’après une neurotomie partielle correctement effectuée » [17]. En 1955, Selverstone cherchera à améliorer la sécurité du geste par une stimulation électrique préalable à l’injection. Ce nouveau procédé — destiné à contrôler surtout le bon positionnement de l’aiguille — n’en diminuera pas moins les complications, mais sera repris pour la thermocoagulation [5].
L’électrocoagulation du ganglion de Gasser
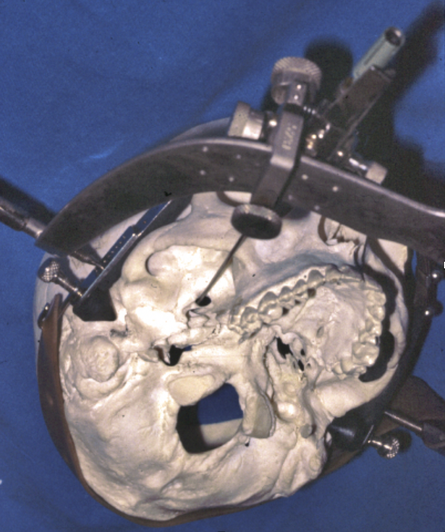
En 1931, bien avant que l’électricité ne soit utilisée à des fins de stimulation, M. Kirschner, à Heidelberg, y recourra pour détruire le ganglion du Trijumeau [37]. Malgré l’appui de la stéréotaxie, cette « électrochirurgie » s’avérera décevante (Fig. 6). « L’électrocoagulation du ganglion de Gasser, déplore Mazars, tel que la technique de Kirschner la réalise est une mauvaise intervention au même titre que toutes celles qui interrompent massivement les voies sensitives trigéminales, mais c’est le mérite de Thiry d’avoir un des premiers réalisé que, sans modification fondamentale de la technique originale de Kirschner, il était possible de réaliser une coagulation limitée, qui ne concerne qu’une petite portion du ganglion de Gasser ou de la racine postérieure tout en conservant une bonne efficacité sur les crises de névralgie faciale » [16]. Malgré l’appui de la stéréotaxie, cette « électrochirurgie » s’avèrera, à ses début, décevante. Kirchner utilisait une aiguille reliée à un générateur de coagulation dont le courant était contrôlé. Il avait, par ailleurs, développé un cadre de stéréotaxie, le premier utilisé chez l’homme, à partir du repérage des trous ovales sur une radiographie en incidence de Hirst, ce qui permettait de ponctionner très précisément le trou ovale. La méthode utilisée a, par la suite, été intégralement reprise par Sweet qui l’avait découverte lors d’un voyage en Europe. Le mérite de Sweet a été de faire développer par B J. Cosman, un générateur par radio fréquence qui permet d’obtenir des lésions plus précises et des aiguilles équipées de thermistance puis de thermocouple permettant de contrôler la température [38]. Kirchner et ses élèves dont Philippidès de Strasbourg avaient défini des critères précis — ne pas enfoncer l’aiguille profondément dans le cavum de Meckel, effectuer des anesthésies itératives par thiopental dont la durée d’action brève permet de vérifier le résultat obtenu après chaque coagulation —, ce qui leur permettait d’obtenir de résultats satisfaisants avec peu de complications [39]. On doit au Liégeois S. Thiry l’idée, en 1962, de recourir, lors de cette électrocoagulation, à un courant de faible ampérage (250 mA). Cette intensité réduite diminuera le risque d’anesthésie totale [40]. Dix ans plus tard, en Allemagne, K. Schürmann préférera, à l’anesthésie générale, la neuroleptanalgésie qui autorise un contrôle en temps réel des effets de cette thermocoagulation. L’Américain W. Sweet, par de nouvelles améliorations et reprenant les précédentes, jettera les bases de la thermocoagulation rétrogassérienne. Le principe de ce geste étant de « réaliser un déficit aussi minime que possible dans le territoire affecté par les crises douloureuses, il faut s’efforcer de ne pas dépasser les limites du contingent rétroganglionnaire correspondant » [22]. Le neurochirurgien du Massachusetts General Hospital effectuera le geste sous neuroleptanalgésie et contrôle radiologique. Après la montée de l’aiguille — suivant la voie de Härtel — dans la portion rétrogassérienne, Sweet, dans un premier temps, effectue une stimulation permettant de s’assurer que les fourmillements induits intéressent le territoire de la névralgie. Le second temps, sous anesthésie générale, consiste en une thermocoagulation soigneusement « monitorée » et menée par pallier de 5 à 10° jusqu’à atteindre 60-70°. Le temps nécessaire pour qu’une lésion « minime, mais efficace » de cette portion rétrogassérienne soit obtenue.
La compression par ballonnet
En 1978, se basant sur les observations de Shelden constatant qu’une compression du ganglion de Gasser donnait des résultats supérieurs à ceux de la décompression, S. Mullan, entreprit de réaliser des compressions du ganglion par voie percutanée [25]. Empruntant également la voie de Härtel, le chirurgien de Chicago effectuera ses « microcompressions » à l’aide du ballonnet d’une sonde de Fogarty. Un fois l’extrémité du trocart à l’entrée du cavum de Meckel, le ballonnet est gonflé par du produit de contraste, jusqu’à en devenir piriforme. Les résultats de la littérature montrent que 97% des patients sont immédiatement soulagés et, dans deux tiers des cas, le demeurent à long terme [41]. L’inconvénient de ce geste, aujourd’hui de pratique courante, réside dans des hypoesthésies dont la fréquence varie considérablement d’une série à l’autre (4 à 77%) et une parésie masticatrice qui concerne plus de la moitié des opérés.
L’injection rétrogassérienne de glycérol
La dernière technique, l’injection de glycérol par voie percutanée dans la citerne trigéminale, doit à la sérendipité de l’équipe de l’Institut du Karolinska. À partir de 1951, L. Leksell et ses collaborateurs ont cherché à mettre au point un traitement radiochirurgical de la névralgie trigéminée. Ce traitement, délivré par les rayons gamma en condition stéréotaxique, impliquait un ciblage radiologique précis. Pour cela les Suédois ont eu recourt à des injections dans le cavum de Meckel d’un produit de contraste — le Tantale — dilué à de la glycérine. Contre toute attente, S. Håkanson remarquera que les patients à qui l’on injectait le glycérol étaient soulagés y compris en l’absence de traitement radiochirurgical [42]. Si les résultats sont satisfaisants — 42 à 84% de sédation immédiate de la douleur avec un effet à long terme de 18 à 59% [41] — cette technique d’injection cisternale expose à des risques du même ordre de ceux de l’alcoolisation du ganglion de Gasser, à savoir, une possible et dommageable diffusion du produit neurolytique dans les espaces sous-arachnoïdiens.
La radiochirurgie
Le traitement de la névralgie faciale par la radiochirurgie vient d’être évoqué avec l’injection de glycérol. Néanmoins, bien avant les travaux de Leksell, le chirurgien allemand H. Gocht proposera, dès 1897, le recours aux radiations ionisantes dans le traitement du tic douloureux [43]. Cet orthopédiste berlinois traitera ainsi une vingtaine de patients par rayons X. Dix sept seront soulagés, des résultats confirmés par d’autres observateurs [44]. En 1951, le neurochirurgien Leksell — déplorant les complications hémorragiques et infectieuses des gestes de psychochirurgie — aura l’idée de pratiquer des lésions cérébrales ciblées par le biais de rayonnements ionisants. Deux ans plus tard, il traitera deux patients en délivrant des rayons X par un tube de 280 kV fixé à un arc solidaire d’un cadre de stéréotaxie. Des malades qui, en 1971, demeuraient soulagés [45]. Rapidement Leksell et son physicien, B. Larsson, remplaceront les rayons X par des protons de hautes énergies [46] puis des rayons Gamma provenant de source de Cobalt [47]. Un rayonnement Gamma qui aura vocation à se substituer, dans certaines indications, au bistouri du chirurgien. Cela deviendra le « Gamma-knife ® ». Vers le milieu des années quatre-vingt-dix, une littérature de plus en plus solide et étoffée ainsi qu’une importante étude multicentrique viendront confirmer l’efficacité et la sécurité du Gamma-Knife dans le traitement de la névralgie du trijumeau [48].
Conclusion
Si l’on recense, depuis un siècle, l’ensemble des variantes de gestes à ciel ouvert ou percutané ce sont plus d’une vingtaine de procédures qui ont été proposées dans le traitement chirurgical de la névralgie faciale. L’avènement de médicaments efficaces a raréfié ces gestes pour ne conserver que les plus efficaces et de moindres complications. Quatre — voir cinq — interventions sont aujourd’hui disponibles en cas d’échec ou d’intolérance du traitement médicamenteux. De celles-ci, la décompression vasculaire est la seule à vocation véritablement curatrice. Elle possède, néanmoins, l’inconvénient d’être la procédure la plus lourde et, de ce fait, réservée à des sujets en bon état général sans contre-indication envers un geste d’anesthésie générale. Pour les autres patients, le choix se portera, selon les écoles, vers la radiochirurgie ou les gestes percutanés : compression par ballonnet, thermocoagulation et — dans une moindre mesure — l’injection de glycérol. Ce panel d’interventions permet dorénavant au praticien de faire face à tous les types de névralgies pour toutes les catégories de patients. Chaque intervention a ses avantages et ses inconvénients. La décision finale revient au patient à qui le médecin aura donné une information loyale, claire et appropriée suivant les termes consacrés.
Références
1. Halliday D (1832) Considérations pratiques sur les névralgies de la face. BiblioBazaar, Paris
2. André N (1756) Observations pratiques sur les maladies de l'urethre, et sur plusieurs faits convulsifs, & la guérison de plusieurs maladies chirurgicales. Delaguette,
3. Eboli P, Stone JL, Aydin S, Slavin KV (2009) Historical characterization of trigeminal neuralgia. Neurosurgery 64 (6):1183-1186; discussion 1186-1187. doi:10.1227/01.neu.0000339412.44397.76
4. Dewhurst K (1957) A symposium on trigeminal neuralgia; with contributions by Locke, Sydenham, and other eminent seventeenth century physicians. Journal of the history of medicine and allied sciences 12 (1):21-36
5. Stookey BP, Ransohoff J (1959) Trigeminal neuralgia: its history and treatment. Thomas,
6. Brown JA, Coursaget C, Preul MC, Sangvai D (1999) Mercury water and cauterizing stones: Nicolas Andre and tic douloureux. Journal of neurosurgery 90 (5):977-981. doi:10.3171/jns.1999.90.5.0977
7. Leriche R (1937) La chirurgie de la douleur. 1. - éd. edn. Masson, Paris,
8. Tubbs RS, Loukas M, Shoja MM, Cohen-Gadol AA (2010) John Murray Carnochan (1817-1887): the first description of successful surgery for trigeminal neuralgia. Journal of neurosurgery 112 (1):199-201. doi:10.3171/2009.5.jns09192
9. Carnochan J (1858) Exsection of the trunk of the second branch of the fifth pair of nerves, beyond the ganglion of Meckel, for severe neuralgia of the face: with three cases. Am J Med Sci 69 (ART. XII)
10. Horsley V (1891) Remarks on the Various Surgical Procedures Devised for the Relief or Cure of Trigeminal Neuralgia (Tic Douloureux). Br Med J 2 (1613):1139-1143
11. Hartley F (1892) Intracranial neurectomy of the second and third divisions of the fifth nerve; a new method. NY Med J 55:317–319
12. Rose W (1892) The Lettsomian Lectures on the surgical treatment of trigeminal neuralgia. Lancet 139 (3571):295-302
13. Spiller W, Frazier C (1901) The division of the sensory root of the trigeminus for relief of tic douloureux; an experimental, pathological, and clinical study, with a preliminary report of one surgically successful case. University of Pennsylvania Medical Bulletin 14:342-352
14. Frazier CH (1928) OPERATION FOR THE RADICAL CURE OF TRIGEMINAL NEURALGIA: ANALYSIS OF FIVE HUNDRED CASES. Ann Surg 88 (3):534-547
15. Cole CD, Liu JK, Apfelbaum RI (2005) Historical perspectives on the diagnosis and treatment of trigeminal neuralgia. Neurosurg Focus 18 (5):E4
16. Mazars G, Cioloca C, Merienne L (1976) Etat actuel de la chirurgie de la douleur: XXVIe congrès annuel, Clermont-Ferrand, 17 - 19 juin 1976. Masson,
17. Guillaume J, de Sèze S, Mazars G (1949) Chirurgie cérébro-spinale de la douleur. Presses universitaires de France,
18. Dandy W (1925) Section of the sensory root of the trigeminal nerve at the pons: preliminary report of the operative procedure. Bull Johns Hopkins Hosp 36:105-106
19. Sjöquist O (1938) Eine neue operationsmethode bei trigeminus neuralgie ; durchschneidung des tractus spinali trigemini. . Zentralblatt Neurochir 2:174
20. Grant FC (1943) Surgical Methods for Relief of Pain. Bull N Y Acad Med 19 (6):373-385
21. Kunc Z (1977) [Modification of trigeminal tractotomy by partial vertical nucleotomy]. Ceskoslovenska neurologie a neurochirurgie 40 (4):201-205
22. Mazars G, Merienne L, Cioloca C (1976) Etat actuel de la chirurgie de la douleur. Neuro-Chirurgie 22:53–61
23. Olivecrona H (1949) Cholesteatomas of the cerebello-pontine angle. Acta psychiat:639-643
24. Taarnhoj P (1952) Decompression of the trigeminal root and the posterior part of the ganglion as treatment in trigeminal neuralgia; preliminary communication. Journal of neurosurgery 9 (3):288-290. doi:10.3171/jns.1952.9.3.0288
25. Shelden CH, Pudenz RH, Freshwater DB, Crue BL (1955) Compression rather than decompression for trigeminal neuralgia. Journal of neurosurgery 12 (2):123-126. doi:10.3171/jns.1955.12.2.0123
26. Dandy W (1966) The brain. In: Lewis D, Walters W, Ellis FH (eds) Lewis-Walters Practice of Surgery. Prior, Hagerstown,
27. Gardner W, Miklos M (1959) Response of trigeminal neuralgia to decompression of sensory root. JAMA : the journal of the American Medical Association 170:1773-1776
28. Janetta P, Rand R (1966) Transtentorial Retrogasserian Rhizotomy MicrosurgicalTechnique» Bull Los Angeles Neurol Soc 31:93-99
29. Provost J, Hardy J (1970) Microchirurgie du trijumeau. 6:459-470
30. Jannetta PJ (2010) Trigeminal Neuralgia. OUP USA,
31. Blom S (1962) Trigeminal neuralgia: its treatment with a new anticonvulsant drug (G-32883). Lancet 1 (7234):839-840
32. Sindou M, Mertens P, Maarrawi J, Kéravel Y (2007) Neurochirurgie de la douleur. EMC (Elsevier Masson SAS, Paris) Neurologie:17-700-B-710
33. Bartholow R (1883) A Practical Treatise on Materia Medica and Therapeutics.
34. Harris W (1912) Three Cases of Alcohol Injection of the Gasserian Ganglion for Trigeminal Neuralgia. Proc R Soc Med 5 (Clin Sect):115-119
35. Härtel F (1914) Über die intracranielle Injektionsbehandlung der Trigeminusneuralgie. Med Klinik 10:582–584
36. Pollock L, Potter H (1916) Experimental studies of injection of the gasserian ganglion controlled by fluoroscopy. JAMA : the journal of the American Medical Association 67:1357–1136
37. Kirschner M (1931) Zur Elektrochirurgie. Arch Klin Chir 167:761–768
38. Sluijter M, Racz G (2002) Technical aspects of radiofrequency. Pain practice : the official journal of World Institute of Pain 2 (3):195-196
39. Philippides D (1953) The neurosurgical treatment of trigeminal neuralgia]. Strasb Med 4 (2):87-92
40. Thiry S, Hotermans J (1974) Traitement de la névralgie essentielle du trijumeau par stéréotaxie et électrocoagulation partielle selective du ganglion de Gasser Neuro-Chirurgie 20 (55-60)
41. Sindou M, Keravel Y, Simon E, P. M (2012) Névralgie du trijumeau et neurochirurgie. . EMC - Neurologie Article 17-023-A-85 (1):1-14
42. Hakanson S (1981) Trigeminal neuralgia treated by the injection of glycerol into the trigeminal cistern. Neurosurgery 9 (6):638-646
43. Bongiovanni A (1907) Alcune applicazioni pratiche della radium terapia alla cura delle paralisi periferiche del faciale e nevralgiedel trigemino. Nuovoapparecchio. Gazzettadegli Ospedalie delle Cliniche 93:962-964
44. Artico M, De Caro GM, Fraioli B, Giuffre R (1997) 1897--celebrating the centennial--Hermann Moritz Gocht and radiation therapy in the treatment of trigeminal neuralgia. Acta Neurochir (Wien) 139 (8):761-763
45. Lozano AM, Gildenberg PL, Tasker RR (2009) Textbook of Stereotactic and Functional Neurosurgery. vol vol. 1. Springer,
46. Leksell L (1971) Sterotaxic radiosurgery in trigeminal neuralgia. Acta Chir Scand 137 (4):311-314
47. Larsson B, Leksell L, Rexed B, Sourander P, Mair W, Andersson B (1958) The high-energy proton beam as a neurosurgical tool. Nature 182 (4644):1222-1223
48. Kondziolka D, Lunsford LD, Flickinger JC, Young RF, Vermeulen S, Duma CM, Jacques DB, Rand RW, Regis J, Peragut JC, Manera L, Epstein MH, Lindquist C (1996) Stereotactic radiosurgery for trigeminal neuralgia: a multiinstitutional study using the gamma unit. Journal of neurosurgery 84 (6):940-945. doi:10.3171/jns.1996.84.6.0940